Оборудование и реагенты
для генетических иследований
для генетических иследований
Наборы реагентов для приготовления библиотек от Twist Bioscience — лидера на рынке NGS
Компания Sesana является официальным поставщиком Twist Bioscience в России и странах СНГ

sales@sesana.ru
Наборы для подготовки библиотек от Twist Bioscience — лидера на рынке NGS
Компания Sesana является официальным поставщиком Twist Bioscience в России и странах СНГ.

Подробнее
Характеристики
Преимущества набора
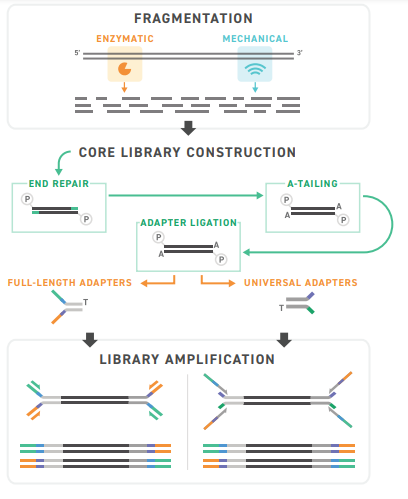
Twist Library Preparation EF Kit (Enzymatic Fragmentation) 2.0 Комплекты для подготовки библиотеки EF Kit 2.0 включает в себя реагенты, необходимые для концевой репарации, безматричного 3'-аденилирования, лигирования адаптера и амплификации библиотеки. Этот набор также включает ферменты для фрагментации образцов гДНК и позволяет настраивать размеры образцов. После создания основной библиотеки можно использовать полноразмерные адаптеры или универсальные адаптеры Twist в соответствии с потребностями пользователя.
Позволяет определять последовательность большего числа образцов за цикл и добиваться более глубокого секвенирования по желаемым целевым областям, сохраняя при этом высокую однородность и низкую частоту отклонений.
Наборы оптимизированы для облегчения подготовки библиотек для последующего секвенирования всего генома, а также целевого обогащения. Совместимы с набором адаптеров Twist Universal Adapter System - для подготовки библиотек с максимальным выходом
Совместимы с набором адаптеров Twist CD Index Adapter - для подготовки библиотеки, используя протокол без стадии ПЦР (PCR-free library preparation )
Совместимы с набором адаптеров Twist CD Index Adapter - для подготовки библиотеки, используя протокол без стадии ПЦР (PCR-free library preparation )
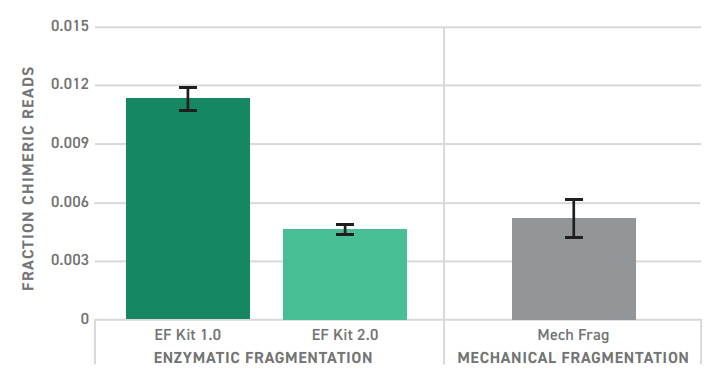
Во время подготовки библиотеки сводятся к минимуму ошибки при лигировании или рекомбинации ДНК, что улучшает качество секвенирования. Обновленный EF Kit 2.0 обеспечивает значительно уменьшенную долю химерных прочтений, по сравнению с EF Kit 1.0. Количество химерных последовательностей, снижено до уровня подготовки библиотек с механической фрагментацией.
Чем меньше химер, тем меньше ошибок секвенирования
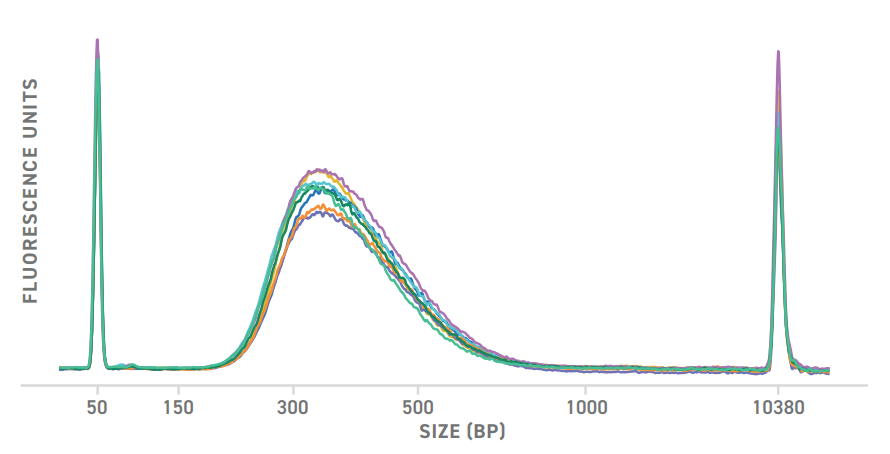
Высокая воспроизводимость, проверенная при валидации тест-набора, гарантирует уверенность в результатах экспериментов. Перекрытие кривых электрофореграмм библиотек NGS, созданных с помощью этого набора, демонстрирует минимальное отклонение между повторами образцов
Высокая воспроизводимость от образца к образцу
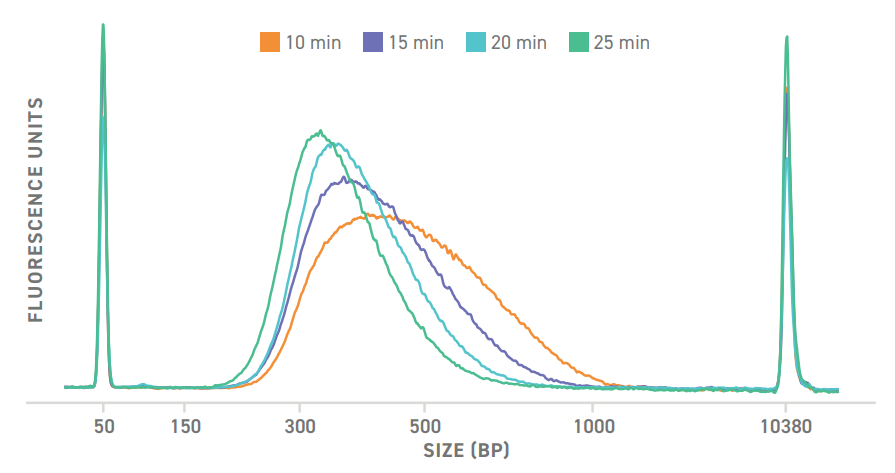
С помощью EF Kit 2.0 размер фрагмента библиотеки ДНК можно настроить в соответствии с вашими конкретными потребностями, просто настроив время фрагментации. Здесь показаны четыре электрофореграммы библиотек NGS, созданные с использованием разного времени фрагментации.
Настройте размер фрагмента в соответствии с потребностями вашего эксперимента
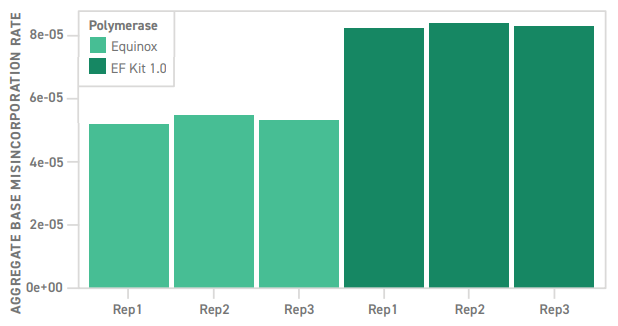
Улучшенная амплификация для минимизации ошибок секвенирования
Ошибки при амплификации неизбежны, но они не обязательно должны становиться рутиной. В состав нового комплекта EF Kit 2.0 входит смесь Equinox Master Mix с высокоточным ферментом для горячего старта. По сравнению с EF Kit 1.0, возникает меньшее количество ошибочно введенных оснований ДНК. Это увеличивает точность амплификации и качество данных секвенирования
Библиотеки NGS собирали с помощью EF Kit 1.0, EF Kit 2.0 или Twist Library Preparation with Mechanical Fragmentation Kit. Для обогащения целевых фрагментов использовали панели Twist Core Exome и системы Twist. Секвенирование выполняли на платформе NextSeq 550 или NextSeq 2000. Планки погрешностей представляют собой стандартное отклонение между повторами.
Восемь библиотек NGS были созданы с помощью EF Kit 2.0 и Twist's Universal Adapter System. 50 нг высококачественной гДНК фрагментировали в течение 20 минут при 37 ° C. Для амплификации использовали шесть циклов ПЦР. Образцы были проанализированы с помощью Agilent DNA 7500, а результаты визуализированы в программе Expert 2100.
Библиотеки NGS были созданы с помощью EF Kit 2.0 и системы универсального адаптера Twist. 50 нг высококачественной гДНК фрагментировали разное время при 37 ° C. Для амплификации использовали шесть циклов ПЦР. Образцы были проанализированы с помощью анализа Agilent DNA 7500, а результаты наложены в программе Expert 2100.
Использовали мастер-миксы для амплификации из EF Kit 1.0 и EF Kit 2.0. Случаи неправильного включения оснований измеряли с помощью запатентованного анализа на основе NGS. Показанные значения представляют собой среднюю частоту ошибок для всех случаев неправильного включения.
Streamline Your Workflow
• Flexible DNA sample input from 1 ng–500 ng
• Convert DNA samples into robust, amplified libraries in three hours
• Single-tube library prep for improved efficiency and consistent results
Robust, High-yield Amplification
• Hot-start enzyme formulation with high efficiency at low input volumes
• High range of GC content tolerance (20–80%) during library preparation
• Improved error rate compared to frequently used polymerases
High Uniformity and Lower Chimera Rate
• Pairs with Twist’s Target Enrichment workflow to enable highly uniform amplification
• Higher confidence in true-chimera detection
• Consistent yield from high-complexity libraries deliver on sensitivity and specificity
• Flexible DNA sample input from 1 ng–500 ng
• Convert DNA samples into robust, amplified libraries in three hours
• Single-tube library prep for improved efficiency and consistent results
Robust, High-yield Amplification
• Hot-start enzyme formulation with high efficiency at low input volumes
• High range of GC content tolerance (20–80%) during library preparation
• Improved error rate compared to frequently used polymerases
High Uniformity and Lower Chimera Rate
• Pairs with Twist’s Target Enrichment workflow to enable highly uniform amplification
• Higher confidence in true-chimera detection
• Consistent yield from high-complexity libraries deliver on sensitivity and specificity
Демонстрация возможностей
Мы готовы предоставить пробные реагенты, продемонстрировать работу наборов на базе нашей лаборатории и провести необходимое обучение. Вы также сможете поработать с образцами перед покупкой.

Профессиональная поддержка
Консультации специалистов, имеющих практический опыт работы с оборудованием, которое мы продаем.
Ведем клиента на всем пути от выбора решения до анализа данных.
Команда опытных сотрудников лаборатории всегда готова проконсультировать по любому вопросу (ведь именно в тот же момент коллеги могут столкнуться с точно такой же задачей, что и Вы).
Дополнительные реагенты:
Доставка от 1 дня
Команда опытных сотрудников лаборатории всегда готова проконсультировать по любому вопросу (ведь именно в тот же момент коллеги могут столкнуться с точно такой же задачей, что и Вы).

Заказать обратный звонок:
Оставьте свои данные
Мы свяжемся с Вами в ближайшее время
Нажимая кнопку, Вы даете свое согласие на обработку Ваших персональных данных

Реагенты и оборудование для
генетических исследований
генетических исследований
г. Москва, Подольское шоссе, дом 8, корпус 5 (метро Тульская)
ООО СЕСАНА, ИНН/КПП 7701412950770101001
Юридический адрес: 105005, г. Москва, ул. Бауманская, 50/12, строение 1.






